فرآیند تولید سلول های زنده از صفر
پژوهشگرها موفق به ساخت سلولهای زندهای شدند که میتوانند انرژی خود را تولید کنند. برای این فرآیند از ترکیب دانش فیزیک و زیستشناسی استفاده شده است.
هشت نوع مادهی اولیه برای این فرآیند لازم است: دو پروتئین، سه عامل بافر، دو نوع مولکول چربی و مقداری انرژی شیمیایی. این موارد برای ساخت یک مجموعه از حبابهای نوسانگر و جهنده (سلول اولیه) لازم هستند که برای تقسیم خود از بعضی دستگاهها استفاده میکنند.
برای پترا اسکویل بیوفیزیکدان، سازههای رقصان آزمایشگاه یک گام مهم به سمت ساخت سلول ترکیبی از صفر هستند؛ او از ده سال گذشته روی این پروژه کار کرده است و اخیرا در مؤسسهی بیوشیمی مکسپلانک در مارتینسرید آلمان به کار خود ادامه میدهد. او میگوید:
همیشه به دنبال پاسخ به این سؤال بودم: چه چیزی یک موجود زنده را از یک موجود غیرزنده متمایز میکند؟
به گفتهی اسکویل چالش اصلی، شناسایی مؤلفههای مورد نیاز برای ساخت یک سیستم زنده است. او معیارهای مستقل تأثیرگذار در یکسلول ترکیبی بینقص را شناسایی کرده است.
پژوهشگرها در تلاشاند تا بیست سال آینده موفق به ساخت سلولهای مصنوعی شوند، آنها از طریق ترکیب بیومولکولها در بافت مناسب به این هدف میرسند. اگرچه این فرآیند ابعاد مختلفی دارد اما میتوان آن را به سه دسته تقسیم کرد: جداسازی بیومولکولها در فضا؛ متابولیسم، یا فرآیند بیوشیمیایی برای زنده ماندن سلول؛ و کنترل اطلاعاتی، ذخیره و مدیریت دستورالعملهای سلولی.
به لطف پیشرفتهای اخیر در فناوریهای میکروسیال سرعت این پژوهشها در حال افزایش است، دانشمندان با استفاده از این فناوریها میتوانند به هماهنگسازی حرکت مؤلفههای کوچک سلولی بپردازند. گروههای پژوهشی قبلا به شناسایی روشهای ساخت حبابهای سلولمانند در شکلهای دلخواه و ساخت نسخههای ناقص از متابولیسم سلولی و شفافسازی ژنومهای دست ساز در سلولهای زنده پرداختهاند؛ اما ترکیب تمام این عناصر هنوز به صورت یک چالش باقی مانده است.
بااینحال میتوان به آیندهی این پژوهشها امیدوار بود. در سپتامبر ۲۰۱۷ پژوهشگرهای ۱۷ آزمایشگاه در هلند گروهی به نام ساخت سلول ترکیبی (BaSyc) را تشکیل دادند که به گفتهی مرلین دوگتروم رییس BaSyC و رییس یک آزمایشگاه در دانشگاه فناوری دلفت، هدف این پروژه ساخت یک سیستم تقسیم و رشد شبه سلولی در طی ده سال است. بودجهی ۱۸.۸ میلیون یورویی این پروژه تحت حمایت Dutch Gravitation تأمین شده است.
 مؤسسهی ملی علوم ایالاتمتحده (NSF) در ماه سپتامبر اولین برنامهی خود برای سلولهای ترکیبی را با سرمایهگذاری ده میلیون دلار اعلام کرد. چند پژوهشگر اروپایی از جمله اسکویل، طرح پیشنهاد خود برای ساخت یک سلول ترکیبی را بهعنوان یکی از طرحهای پرچمدار و نوظهور ارائه دادند و این طرح هم با سرمایهگذاری ۱ میلیارد یورویی اجرا خواهد شد. بر اساس پیشبینی زیستشناسهای ترکیبی، اولین سلولهای کاملا مصنوعی در کمتر از ده سال میتوانند به سلولهای زنده تبدیل شوند.
مؤسسهی ملی علوم ایالاتمتحده (NSF) در ماه سپتامبر اولین برنامهی خود برای سلولهای ترکیبی را با سرمایهگذاری ده میلیون دلار اعلام کرد. چند پژوهشگر اروپایی از جمله اسکویل، طرح پیشنهاد خود برای ساخت یک سلول ترکیبی را بهعنوان یکی از طرحهای پرچمدار و نوظهور ارائه دادند و این طرح هم با سرمایهگذاری ۱ میلیارد یورویی اجرا خواهد شد. بر اساس پیشبینی زیستشناسهای ترکیبی، اولین سلولهای کاملا مصنوعی در کمتر از ده سال میتوانند به سلولهای زنده تبدیل شوند.
همه چیز در یک بسته
گروههای پژوهشی گامهای بلندی را در جهت بازسازی ابعاد مختلف زندگی شبهسلولی برداشتهاند برای مثال میتوان به اقداماتی مثل شبیهسازی غشاهای دور سلولی و تقسیمبندی مؤلفههای داخلی آن اشاره کرد. نکتهی مهم در سازماندهی مولکولها همکاری آنها در زمان و مکان مناسب است به همین دلیل نیاز به فرآیند تقسیمبندی است.
برای مثال میتوان یک میلیارد باکتری را داخل محتویات یک لولهی تست ریخت اما فرآیندهای بیولوژیکی مدت زیادی دوام نمیآورند. بعضی مؤلفهها باید به صورت جدا و بعضی با هم نگهداری شوند. به گفتهی سی دکر بیوفیزیکدان دانشگاه فناوری دلفت، در این بخش اجتماع مولکولها مهم است.
مهمتر از هرچیز این فرآیند به معنی سازماندهی مولکولهای زیستی داخل یا روی غشاهای لیپیدی است. اسکویل و تیم او در زمینهی غشا تخصص دارند. تقریبا یک دهه پیش، این تیم فرآیند اضافه کردنپروتئینهای Min را شروع کرد، این پروتئینها دستگاه تقسیم سلول باکتریایی را به صفحات غشای مصنوعی ساختهشده از لیپید هدایت میکند.
به گفتهی پژوهشگرها Min-ها به سرعت وارد غشاها میشوند و باعث حرکت و نوسان آنها میشوند؛ اما به گفتهی اسکویل در صورت اضافه کردن Min-ها به کرههای سهبعدی لیپیدی، ساختار آنها مثل حبابهای صابونی میترکد. گروه اسکویل توانستند با استفاده از روشهای میکروسیال و ساخت نگهدارندههای غشایی در اندازهی سلولی یالیپوزومها بر این مشکل غلبه کنند، زیرا این لیپوزومها در مقابل درج پروتئینهای مختلف مقاوم هستند.
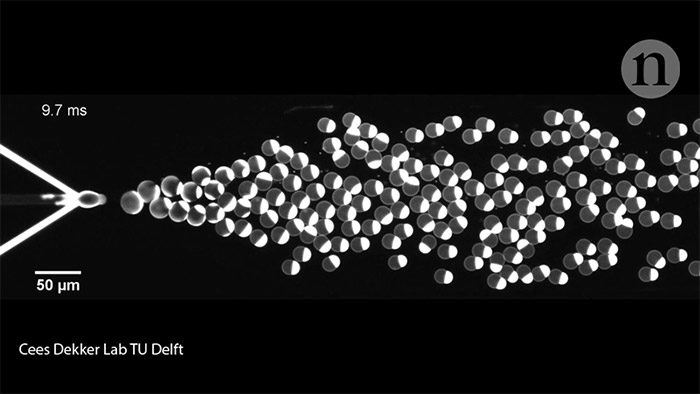
لیپوزومهایی به اندازهی سلول روی یک تراشهی میکروسیال ایجاد شدهاند.
توماس لیچل یکی از دانشجویان اسکویل به همراه همکاران موفق به حل پروتئینهای Min در آب شدند و قطرههایی از این ترکیب را در یک لولهی تست چرخان وارد کردند. نیروی گریز از مرکز قطرهها را به سمت لایههای لیپیدی متراکم کشاند و آنها را در این مسیر به صورت کپسول درآورد. بر اساس نتایج اندازهگیری، عرض لیپوزومها به ۱۰ الی ۲۰ میکرومتر میرسد (تقریبا هم اندازهی یک سلول گیاهی یا حیوانی متوسط). لیپوزومهای حاصل موسوم به واسطههای تک لایهای غولآسا (GUV-ها) را میتوان به روشهای مختلف تولید کرد اما در روش لیچل پروتئینهای Min باعث حرکت، نوسان و انقباض GUV-ها شدند. هدف گروه اسکویل، سرمایهگذاری بر پروتئینهایی است که میتوانند الگوهای غشایی را تولید کند. او میگوید:
ما این مولکولها را خیلی خوب درک میکنیم و باید دید با عناصر نسبتا ساده مثل Min-ها تا کجا میتوانیم پیش برویم.
طبق پروژهی لیچل، میتوان از این پروتئینها برای قالبگیری غشاها و تقسیمبندی استفاده کرد یا مؤلفهها را در یک سمت سلول ترکیبی جمعآوری کرد. همانطور که بعضی فیزیکدانها از نوار لولهای و ورق قلعی برای آزمایشهای خود استفاده میکنند، اسکویل امیدوار است مولکولهای بیولوژیکی سودمند توانایی تعمیر ساختارهای شبه سلولی را داشته باشند.
اعضای تیم دکر هم لیپوزومها را با استفاده از تراشهی میکروسیال با پروتئینهای مورد علاقهی خود پر کردهاند. دو کانال حاوی مولکولهای لیپیدی روی تراشه در یک کانال آبی همگرا میشوند و فرآوردهی حاصل لیپوزومهایی در اندازهی سلولی است که میتوانند از طریق نفوذ به غشا یا شناور شدن داخل محفظه، مولکولهای زیستی را حفظ کنند.
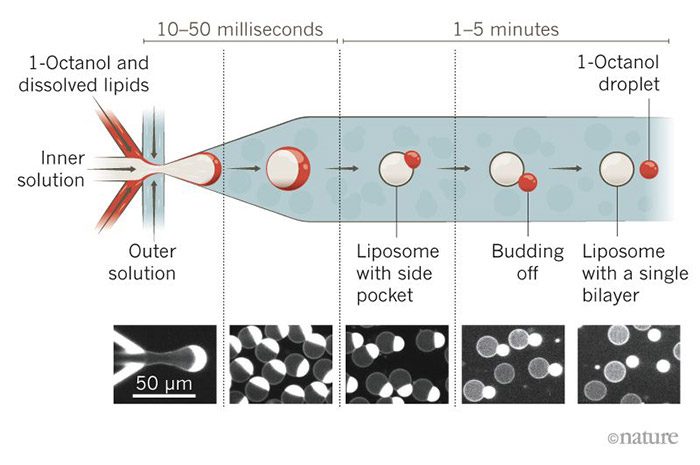
ماشینهای حبابی: پژوهشگرها از تراشههای میکروسیال برای ساخت حبابهای لیپیدی یا لیپوزوم استفاده کردند، لیپوزومها شبیه پوششهایی هستند که سلولها را در خود نگه میدارند. این روش شامل یک اتصال شش جهته است که لیپوزومها را با محلول پر میکند و سپس تخلیه میکند. یک لایهی مضاعف لیپیدی با الکل چرب ۱ اکتانول در ترکیب، حول محلول داخلی شکل میگیرد. به مرور زمان لیپیدهای اضافه و مخزن ۱ اکتانول در یک جهت جدا میشوند و لیپوزوم کامل را به جا میگذارند.
گروه دکر آزمایش را با تنظیم فشار، تغییر شکل لیپوزومها به شکلهای غیرکرهای و شبیه سلولها انجام داد. دستگاههای میکروسیال با استفاده از کانالهای میکرو، امکان کنترل بیشتر برای مرتبسازی و تغییر لیپوزومها را فراهم میکنند، رفتار این کانالها مشابه مدار است. امسال آزمایشگاه دکر تراشهای را طراحی کرده است که میتواند یک لیپوزوم را به یک نقطهی تیز هل دهد و به این صورت آن را برش بزند. دکر میگوید:
البته این تنها هدف ما نیست، بلکه هدف نمایش تقسیمبندی از داخل است اما این آزمایش هم اطلاعات جذابی را فراهم میکند.
مثالها شامل نیروی لازم برای تقسیم سلول و انواع ویرایشهای فیزیکی قابلتحمل برای لیپوزومها هستند. تیم دکر در کنار این فرآیندها به بررسی شکل سلولهای زندهی اشریشیا کلی پرداختند و با پرورش آنها در محفظههای سیلیکونی نانو فابریک آنها را عریضتر میکنند. به این صورت اعضای تیم میتوانند تأثیر شکل سلول بر دستگاه تقسیم را ببینند و عملکرد پروتئینهای Min را در سلولهایی با اندازه و شکل متفاوت ارزیابی کنند. دکر میگوید:
ما با روشهای نانوفابریک سرو کار داریم و کارهایی را انجام میدهیم که یک زیستشناس معمولی قادر به انجام آن نیست؛ اما یک بیوفیزیکدان مانند من از عهدهی این کار برمیآید.
اضافه کردن انرژی به سیستم
در این مرحله میتوان مؤلفهها را بدون تخلیه به حبابهای لیپوزومی اضافه کرد و به بررسی همکاری مولکولها با یکدیگر پرداخت. تقریبا هر عنصر شبه زنده معمولا به انرژی سلولی به شکل ATP نیاز دارد؛ و اگرچه میتوان این انرژی را از خارج به یک سیستم ترکیبی وارد کرد، اما به عقیدهی بسیاری از زیستشناسها یک سلول ترکیبی هم مانندمیتوکندری سلول حیوان یا کلروپلاست گیاه (که هردو ATP تولید میکنند) باید قادر به تولید انرژی مورد نیاز خود باشد.
گروه یوآخیم اسپاتز در مؤسسهی پژوهش پزشکی مکس پلانک هایدلبرگ آلمان موفق به ساخت یک میتوکندری مضاعف شده است که قادر به تولید ATP است. در این پروژه از روشهای جدید میکروسیال استفاده شده است. آنها در ابتدا با قرار دادن GUV-ها در قطرههای آب روغن (که با دیوارههای چسبناک پلیمری احاطه شدهاند) به پایدارسازی آنها پرداختند. پس از جاری شدن GUV-ها روی یک میکروکانال، پروتئینهای بزرگ به داخل آنها (داخل کیسه یا در سطح غشا) تزریق کردند.
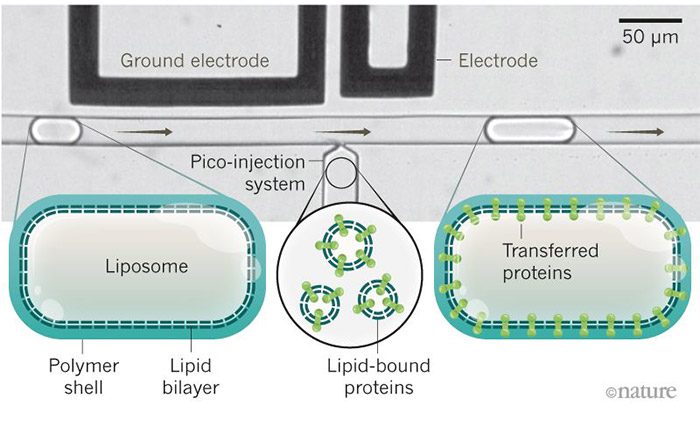
خطوط مونتاژ: یک سیستم تزریق پیکو امکان بارگذاری تقسیمهای شبه غشای سلولی به نام لیپوزوم را با پروتئینهای عملیاتی فراهم میکند. لیپوزومها با یک پوشش پلیمری پایدار میشوند و به یک کانال میکروسیال وارد میشوند. در طول انتقال لیپوزومها روی یک موقعیت تزریق پیکو، یک پالس الکتریک میتواند اتصال پروتئینهای داخلی یا پروتئینهای غشا در لیپوزوم را ایجاد کند.
آنها این غشاها را با یک آنزیم به نام سنتز ATP بارگذاری کردند این آنزیم مانند یک نوع چرخهی آبی مولکولی عمل میکند و انرژی ATP را از مولکولهای پیشرو به صورت جریان پروتونی در کل غشا تولید میکند. با اضافه کردن اسید برای افزایش پروتونهای داخل GUV، ATP تولید میشود.
به گفتهی اسپاتز پژوهشگرها میتوانند GUV-ها را حول میکروکانال برای یک تزریق پروتئینی دیگر به چرخش درآورند و مؤلفهها را به ترتیب اضافه کنند. برای مثال، مرحلهی بعدی میتواند اضافه کردن یک مؤلفه باشد که به صورت خودکار طیف پروتئینی را برای سیستم تنظیم میکند. به گفتهی اسپاتز اهمیت این ماژول به اندازهی یک ماژول واقعی است.
یک گروه ترکیبی زیستشناسی دیگر در مکس پلانک تحت رهبری شیمیدانی به نام توبیاس ارب از روشهای دیگری برای توسعهی مسیرهای متابولیک سلولی استفاده میکند. در روش این گروه میکروبهای فوتوسنتزی، کربن دیاکسید محیط را جذب میکنند و قند و دیگر بلوکهای سلولی را میسازند.
ارب، رهبر گروه مؤسسهی مکس پلانک در بخش میکروبیولوژی ماربورگ آلمان، از روش لوح خالی برای ترکیب مسیرهای متابولیکی سلولی استفاده میکند. او میگوید:
از دیدگاه مهندسی، ما به روش طراحی فکر میکنیم و سپس آن را در آزمایشگاه میسازیم.
آنها موفق به طراحی سیستمی شدند که قادر است Co2 را به نمک اسید مالیک تبدیل کند، این ماده یکی از متابولیتهای کلیدی در طول فتوسنتز است. طبق پیشبینی این فرآیند از فتوسنتز هم بهینهتر است. ارب و همکاران او در مرحلهی بعد به جستوجوی آنزیم در پایگاه داده پرداختند این نوع آنزیم قادر است هر واکنشی را اجرا کند. برای این کار آنها میبایست آنزیمهای موجود را به آنزیمهای طراح تبدیل میکردند.
آنها در پایان ۱۷ آنزیم را از ۹جاندار مختلف از جمله E.coli، آرکائون (یک نوع جاندار میکروبی)، گیاه آرابیدوپسیس و انسان پیدا کردند. این فرآیند بهینه اما کند بود. به گفتهی ارب، گروهی از آنزیمها کنار هم قرار داده شدند اما در کنار هم عملکرد خوبی نداشتند. آنها پس از مهندسی آنزیمها به یک نسخهی ۵.۴ رسیدند که به گفتهی ارب ۲۰ درصد بهینهتر از فتوسنتز است.
به این ترتیب گروه ارب ساخت یک نسخهی خام از کلروپلاست ترکیبی را شروع کردند. آنها در ابتدا اسفناج را در یک مخلوطکن پودر کردند و سپس ماشین فتوسنتز را به سیستم آنزیمی آن در لولهی تست اضافه کردند، در این فرآیند ATP تولید شد و توانستند Co2 را به نمک اسید مالیک تبدیل کنند (با تابش نور فرابنفش به آن).
اگرچه آزمایش برای مدت کوتاهی در لولهی تست خوب پیش میرود اما ارب میخواهد ترکیب را مانند یک کلروپلاست تقسیمبندی کند. به این منظور از کیت آدامالا زیست شناس ترکیبی کمک گرفت که میتواند بخشهای پیچیده را بسازد و کنترل کند.
گروه آدامالا در دانشگاه مینسوتای میناپولیس با معرفی مدارهای ژنتیکی ساده در لیپوزومها و ترکیب آنها با یکدیگر و ساخت بیورآکتورهای پیچیدهتر روی بیورآکتورهای قابل برنامهریزی کار میکنند. به گفتهی آدامالا، بیورآکتورها، حبابهای صابونی هستند که در ساخت پروتئین نقش دارند.
گروه او بیورآکتورها را با استفاده از یک سیستم لولهای چرخان مشابه نمونهی اسکویل میسازد اما این نمونه لیپوزومهای کوچکتری را تولید میکند. پژوهشگرها در این آزمایش دایرههای DNA موسوم بهپلاسمیدرا اضافه کردهاند که برای یک عمل مشخص همراه با دستگاههای ساخت پروتئین از DNA طراحی شدهاند.
برای مثال آنها موفق به ساخت بیورآکتورهای لیپوزومی شدند، این بیورآکتورها میتوانند یک آنتیبیوتیک را در محیط خود از طریق روزنههای غشایی حس کنند و در پاسخ یک سیگنال درخشان تولید کنند.
با ترکیب بیورآکتورهای ساده میتوان مدارهای ژنتیکی پیچیدهتری را ساخت؛ اما وقتی سیستم توسعه پیدا میکند، به چند قسمت تقسیم میشود تا بتواند مؤلفههای بیشتری را دربر بگیرد. به گفتهی آدامالا این یک چالش بزرگ است. در یک سلول واقعی، ممکن است پروتئینها در کارهای یکدیگر تداخل ایجاد کنند به همین دلیل با مکانیزمهای مختلف جدا نگه داشته میشوند.
زیستشناسها برای سلولهای ترکیبی سادهتر باید روشهای کنترلی دیگری را پیدا کنند. در این روش آزمایشکننده تصمیم میگیرد کدام لیپوزومها و در چه زمانی با یکدیگر ترکیب شوند. این کار را میتوان از طریق برچسبهای شیمیایی هم انجام داد، این برچسبها نشان میدهند کدام لیپوزومها را میتوان با یکدیگر ترکیب کرد یا تنظیم لیپوزومها را از طریق یک سیستم زمانی انجام میدهند.
تزریقهای اطلاعاتی
مرحلهی بعدی تولید سلول دستیابی به نرمافزار مناسب است. برای این که سلول ترکیبی بتواند دستورالعمل دانشمندان را اجرا کند، به یک فرآیند ذخیره و بازیابی اطلاعات نیاز دارد. برای سیستمهای زنده میتوان از ژنها کمک گرفت (از صدها ژن برای تعدادی میکروب تا دهها هزار ژن برای انسانها).
تعداد ژن مورد نیاز برای راهاندازی سلول ترکیبی به سلامت سلول وابسته است. اسکویل و همکاران تعداد چند هزار ژن را مناسب میدانند درحالیکه به عقیدهی آدامالا سلولهای ترکیبی به ۲۰۰ تا ۳۰۰ ژن نیاز دارند.
بعضی پژوهشگرها روی موجودات زنده کار میکنند. زیستشناس ترکیبی جان گلاس و همکارش در مؤسسهی جی. کریگ ونتر (JCVI) در کالیفرنیا کوچکترین ژنوم میکروبی شناخته شده از کوچکترین ژنومهای میکروبی شناختهشده استفاده کردند (مایکوپلاسما مایکوییدها) و برای شناسایی ژنهای ضروری به جداسازی ژنهای آن پرداختند. با دستیابی به این اطلاعات، موفق به ساخت یک ژنوم مینیمال در آزمایشگاه شدند.
این ژنوم ترکیبی، از ۴۷۳ ژن تشکیل شده است (نیمی از آنها در موجود زنده قرار دارند) و به گونههای باکتری موسوم به مایکوپلاسما کاپری کولوم پیوند زده شده است. بر اساس پژوهشها در سال ۲۰۱۶ ژنوم ترکیبی مینیمال میتواند به (هرچند با رشد کند). به عقیدهی گلاس کاهش تعداد ژنها دشوار است زیرا حذف یک ژن میتواند منجر به مرگ سلولها یا کند شدن رشد آنها نزدیک به صفر شود.
گلاس و همکارانش در JCVI به گردآوری فهرستی از وظایف سلولی بر اساس آخرین نسخهی تولید آنها یعنی JCVI-syn3.0aمیپردازند که میتوانند مشابه یک لیست وظیفهی مینیمال سلولی عمل کنند؛ اما برای ۱۰۰ ژن نتوانستند به شناسایی عملکرد ضروری آنها بپردازند.
در مرحلهی بعد گلاس و آدامالا تحت پشتیبانی NSF و سرمایهی ۱ میلیون دلاری، به نصب ژنوم JCVI-syn3.0a در یک لیپوزوم ترکیبی پرداختند و دوام آن را بررسی کردند، این لیپوزوم شامل دستگاههایی برای تبدیل DNA به پروتئین است. در این نمونه نرمافزار و سختافزار سلول از ابتدا ترکیبی هستند.
اگر سلول قادر به رشد و تقسیم باشد، این آزمایش یک گام بزرگ در نوع خود خواهد بود؛ اما به عقیدهی بسیاری، یک سیستم زنده باید مراحل تکامل را بگذراند و خود را با محیط تطبیق دهد. به گفتهی اسکویل این هدف با نتایج غیرقابل پیشبینی و بزرگترین چالشها همراه است:
تنها زندگی سلول اهمیت ندارد بلکه یک سلول برای رسیدن به حیات، باید یک قابلیت جدید را توسعه دهد.
تیم گلاس در JCVI آزمایشهای تکامل تطبیقی را با JCVI-syn3.0a انجام دادند و به این منظور جاندارانی را انتخاب کردند که در یک محیط مغذی رشد سریعتری دارند. آنها پس از ۴۰۰ تقسیم به سلولهایی رسیدند که رشد آنها ۱۵ درصد سریعتر از رشد جاندار اصلی بود؛ اما هیچگونه شواهدی در مورد توسعهی عملکردهای جدیدی سلولی یا افزایش تناسب آنها از طریق جهش یا نوسان وجود نداشت.
به گفتهی ارب اضافه کردن تکامل به سلولهای ترکیبی تنها راه افزایش جذابیت آنها است. بینظمی اندکی که در سیستمهای زیستی وجود دارد امکان بهبود عملکرد را فراهم میکند. ارب میگوید:
ما بهعنوان مهندس نمیتوانیم یک سلول ترکیبی بینقص را بسازیم بلکه باید یک سیستم خودتصحیح بسازیم که روز به روز بهتر میشود.
سلولهای ترکیبی میتوانند به جستوجوی حیات در سیارههای دیگر کمک کنند. بیورآکتورهای ترکیبی میتوانند تحت کنترل کامل پژوهشگرها راهحلهای جدیدی را برای درمان سرطان، برطرف کردن حساسیتآنتیبیوتیک یا پاکسازی مکانهای سمی ارائه کنند. انتشار یک موجود زنده در بدن انسان یا محیط ممکن است با خطراتی همراه باشد، اما یک جاندار مهندسیشده به روش بالا به پائین با رفتارهای غیرقابل پیشبینی و ناشناخته از این هم خطرناکتر است.
به گفتهی دوگتروم سلولهای ترکیبی زنده سؤالهای اخلاقی و فلسفی را به دنبال دارند: آیا این زندگی واقعی است؟ آیا این استقلال و خودمختاری است؟ آیا میتوان آن را کنترل کرد؟ این بحثها بین دانشمندان و عموم مردم رواج پیدا میکنند. حتی دوگتروم در مورد کشتن انسانها توسط سلولهای ترکیبی نگرانی کمتری دارد و میگوید: من معتقدم اولین سلول ترکیبی ما تقلیدی ضعیف از نمونهی اصلی است.
او به همراه زیستشناسان ترکیبی دیگر به پژوهش خود در مورد حیات ادامه میدهند. او میگوید:
زمانبندی صحیح است ما ژنومها و لیست اجزا را داریم. سلول مینیمال تنها به چند صد ژن نیاز دارد تا به یک نوع زنده تبدیل شود. صدها ژن هم یک چالش بزرگ است اما بسیار هیجان انگیز است.

